GRUPO DE PRÁTICAS 2022_2
GRUPO 1: Grazielle Ribeiro dos Santos, Letícia lima de Sousa. Lyandra de Castro Conceiçãoe Maria Naiara dos Santos Sousa Acesse o LINK aqui
GRUPO 2:
GRUPO 3:
GRUPO 4:
GRUPO 5:
GRUPO 6:
GRUPO DE PRÁTICAS 2022_1
GRUPO 1: Ana Alice, Amanda Cavalcante,Lara Ribeiro, Maria Eulalia, Maria Eduarda, Mateus Oliveira, Naomy Vitória e Virginia Duarte Acesse o PORTIFÓLIO aqui
GRUPO 2: Amanda Santos Barros, Ana Clara Laundos Oliveira, Ana Karoline Mota da Silva, Ana Elizia Denadai Resende, Andressa Barros Farias de Melo, Nicoly de Oliveira e Sara Laís Costa. Acesse o PORTIFÓLIO aqui
GRUPO 3: Ana Gabriela, Juan Pablo, Kaio Samuel, Kyara Moura, Laís da Silva, Letícia Nascimento, Marcos Vinicius. Acesse o Blog do Portifólio aqui
GRUPO 4: Paulina Almeida, Beatriz Silva, Ryan Sousa, Matheus Porto, João Gabriel Rodrigues, Thaiuly Silva e Hávilla Mísia Acesse o BLOG do grupo aqui
GRUPO 5: Vitoria Tatiana Da Silva, Isabella Cordeiro Gomes, Eduarda Costa Santos, Eduarda de Sousa Félix, Carlos Arthur, Ana Caroline Sousa Acesse o Instagram do grupo aqui
GRUPO 6: Francisca Vitória Damasceno Nascimento, Bruna VillaNova, Vinicius Ribeiro, Jada Maria Silva Rodrigues, Bruna Queiroz e Manoel Eduardo. Acesse o Blog do grupo aqui
ROTEIROS DE PRÁTICAS
01_INTRODUÇÃO AO LABORATÓRIO DE BIOQUÍMICA
02_PREPARO DE SORO FISIOLÓGICO
03_COLETA DE SANGUE VENOSO
04_PRESSÃO OSMÓTICA E HEMÓLISE
05_TEMPO DE SANGRAMENTO Acesse o Vídeo aqui
06_PROVA DO LAÇO
07_TESTE DA GLICEMIA
08_TITULAÇÃO ÁCIDO-BASE
09_DETERMINAÇÃO VELOCIDADE E TEMPO DE EFUSÃO DE MEDICAMENTOS
10_BIOQUÍMICA DA URINA
11_DILUIÇÃO SERIADA
12_AMOSTRAS DE SANGUE E ANTICOAGULANTE Acesse o vídeo aqui
13_COAGULAÇÃO SANGUÍNEA Acesse o vídeo aqui
LABORATÓRIO (Francês “Laboratorie”) - Lugar destinado ao estudo experimental de qualquer ramo da ciência, ou à aplicação dos conhecimentos científicos com objetivos práticos, como realização de exames e/ou produção de reagentes químicos e biológicos.
EQUIPAMENTOS
|
· Agitador de frasco (mesa), e de tubo · Agitador magnético · Analisador automático · Autoclave · Balanças semi-analítica e analítica · Banho-maria · Bico de Bunsen · Centrífuga · Cromatógrafos
|
· Deionizador de água · Destilador de água · Estufa de secagem · Espectrofotômetron · Forno Pasteur · Fotocolorímetro · Fotômetron de chama · Freezer · Geladeiras · pH-metron
|
VIDRARIAS
|
· Ampola de decantação · Balão de fundo chato · Balão volumétrico · Becker · Bastão de vidro · Bureta · Cadinho · Cápsula de porcelana · Erlenmayer |
· Funil de separação de vidro · Kitassato · Proveta graduada · Pipeta graduada · Pipetas volumétricas · Tubos de ensaios · Grall com pistilos |
KITS DE DOSAGEM
|
· Dosagem de glicose · Dosagem de colesterol · Dosagem de bilirrubina · Fosfatase alcalina · Transaminases (TGO e TGP) · Dosagem de proteínas
|
· Dosagem de cálcio · Dosagem de Potássio · Dosagem de hemoglobina · Dosagem de uréia · Dosagem de creatinina · Ferro sérico e Ferritina
|
DIVERSOS
|
· Alça de platina · Algodão cardado · Algodão hidrófilo · Barbante · Bulbo de borracha p/ pipeta Pasteur · Cilindros de aço (p/placas, e p/ pipetas) · Espátula · Estante para tubos de ensaio · Etiqueta adesiva. · Filtro milipore
|
· Galeria para tubo de ensaio · Grampo para grampeador · Lâmina de vidro · Luva descartável. · Papel de embrulho · Parafilme · Pinça · Ponteira para pipeta automática · Recipiente para coleta de material. · Swab estéril. cx. 100un. · Tripé |
PROCEDIMENTOS BÁSICOS
1 - PREPARO DE SOLUÇÕES E REAGENTES
2 - DILUIÇÕES SERIADAS
3 - TITULAÇÃO ÁCIDO-BASE
4 - DOSAGEM BIOQUÍMICA
5 - CROMATOGRAFIA
6 - ELETROFORESE
7 - DETERMINAÇÃO PH
8 - COLORIMETRIA – FOTOMETRIA – ESPECTROFOTOMETRO
9 - DENSIDOMETRIA
Biomarcadores ou marcadores biológicos são entidades que podem ser medidas experimentalmente e indicam a ocorrência de uma determinada função normal ou patológica de um organismo ou uma resposta a um agente farmacológico.
1. Biomarcadores da função hepática: Albumina (sangue), Fosfatase alcalina (sangue), Bilirrubinas (sangue) e Aspartato aminotransferase (sangue).
2. Biomarcadores da função renal: Urina de rotina, Uréia (urina), Creatinina (sangue ou urina e Proteinúria 24 horas (urina).
3. Biomarcadores da função cardíaca: Creatinoquinase (sangue), Mioglobina (sangue) e Troponinas (sangue), Homocisteína (sangue).
4. Biomarcadores do metabolismo da glicose: Glicemia de jejum e após sobrecarga (sangue), Lactato (sangue), Hemoglobina glicada (sangue) e Insulina (sangue).
5. Biomarcadores da função da tireóide: T3 total (sangue), T4 livre (sangue), T4 total (sangue) e TSH (sangue).
6. Biomarcadores do metabolismo lipídico: Colesterol total (sangue), Lipoproteína de alta e baixa densidade (sangue), Apolipoproteína A-1 (sangue) e Apolipoproteína B (sangue).
7. Biomarcadores de fase aguda: Proteína C- reativa (sangue), Interleucinas (sangue), Velocidade de hemossedimentação (sangue) e Fator de necrose tumoral (sangue).
8. Biomarcadores do metabolismo ósseo: Ferro (sangue), Cálcio (sangue), Vitamina D (sangue) e Paratormônio (sangue).
9. Biomarcadores do equilíbrio hidroeletrolítico: Sódio (sangue), Potássio (sangue), Magnésio (sangue) e Cloretos (sangue).
10. Biomarcadores do equilíbrio acido-básico: Potencial hidrogeniônico (pH) (sangue ou urina), Pressão parcial de oxigênio (sangue), Pressão parcial de gás carbônico (sangue) e Íons bicarbonato (sangue).
11. Eletroforese de proteínas: Albumina (sangue), Alfa globulina (sangue), Beta globulina (sangue) e Gama globulina (sangue).
12. Biomarcadores do metabolismo do ferro: Ferro sérico (sangue), Transferrina (sangue), Hepcidina (sangue) e Hemossiderina (sangue).
13. Biomarcadores das anemias macrocíticas: Vitamina B12 (sangue), Ácido fólico (sangue), Homocisteína (sangue) e Ácido metilmalônico (sangue).
14. Biomarcadores da função reumática: Fator antinuclear (sangue), Fator reumatóide (sangue) e Anticoagulante lúpico (sangue).
15. Bioquímica do líquido cefalorraquidiano: Proteínas totais (LCR), Lactato (LCR), Glicose (LCR) e Cloretos (LCR).
16. Biomarcadores da desnutrição: Albumina (sangue), Transferrina (sangue), Balanço nitrogenado (sangue) e Proteína transportadora do retinol (sangue).
17. Biomarcadores da função pancreática: Lipase (sangue), Alfa-amilase (sangue ou urina) e Relação da depuração de amilase pela depuração de creatinina (sangue).
18. Biomarcadores da função pulmonar: Alfa-1-antitripsina (sangue) e Dímero D (sangue).
PRÁTICA: Preparo de soro fisiológico
Objetivo: Preparar a solução fisiológica
Princípio: O soro fisiológico é uma solução salina, isotônica em relação aos líquidos corporais, estéril e com aplicação em medicina. Contém 0,9% de NaCl (cloreto de sódio) em massa, dissolvidos em água destilada, ou seja, em 100ml de solução aquosa encontram-se presentes 0,9g do sal. Desta forma, a cada 100ml de soro fisiológico, 0,354g de Na + (sódio) e 0,546g de Cl - (cloro) estarão contidos, em um pH igual a 6,0.
Material: Cloreto de sódio, balança semi-analítica, espátula, erlenmayer de 250ml
Método: Calcular a massa do sal (cloreto de sódio) equivalente para se preparar 150ml da solução, pesar, adicionar no frasco e completar o volume com água destilada para 150ml, agitar para dissolver, transferir para um frasco, rotular e guardar a temperatura ambiente.
Interpretação: A solução fica transparente, límpida, inodora, e quando adicionada uma gota de sangue, não ocorre hemólise, pois se trata de uma solução isotônica.
Comentários: O soro fisiológico é uma solução que contém 0,9% de cloreto de sódio, um tipo de sal, e água estéril, semelhante à concentração de sódio no sangue e em outros fluidos corporais, como lágrima e suor, por exemplo. Geralmente, o soro fisiológico é usado em grandes volumes para fazer infusão na veia em hospitais nos casos de diminuição de líquidos ou sal no organismo ou em pequenas quantidades para diluir remédios para serem aplicados na veia ou no músculo. Além disso, o soro fisiológico 0,9% pode ser usado para fazer limpeza de feridas, lavar os olhos ou para fazer nebulizações, por exemplo, sendo vendido em farmácias, drogarias ou supermercados e comprado sem receita médica.
PRÁTICA: Coleta de sangue venoso
Objetivo: Coletar sangue venoso para realizar exames laboratoriais
Princípio:. Indispensável na maioria dos diagnósticos, a coleta de sangue venoso é fundamental para identificar processos patológicos. O teste de laboratório com amostra de sangue é decisivo na tomada de decisão do médico, que pode indicar o tratamento correto para o problema.
Os exames laboratoriais com coleta de sangue têm o objetivo de diagnosticar, monitorar ou acompanhar o tratamento de uma doença, e são realizados por solicitação médica. Para garantir a qualidade e a confiabilidade dos resultados, é preciso que haja padronização dos processos e controle de qualidade, incluindo a aquisição de materiais para coleta de sangue.
Material: Os materiais médicos necessários são: 1 par de luvas de procedimento; 2 bolas de algodão; 5 mL de álcool a 70%; 1 scalp nº 21 ou 23, ou agulha 30x06 ou 30x07; 1 garrote; uma seringa de 10 mL e tubos para a coleta de sangue de acordo com o pedido médico.
Método: Antes de iniciar o procedimento, o profissional deve orientar o paciente sobre a coleta de sangue venoso e explicar como será feita. Em seguida, deve-se analisar o tubo da amostra de sangue, identificando o nome e o documento do paciente, a data e a hora do exame.
Após verificar se os materiais hospitalares estão todos em conformidade, deve-se higienizar as mãos e calçar as luvas de procedimento. Em seguida, posicionar o paciente sentado em uma poltrona com encosto e descanso para os membros superiores. O braço dele deverá estar sobre o descanso da cadeira, inclinado para baixo e estendido, sendo que o cotovelo não pode estar dobrado.
Em seguida, realiza-se a assepsia do local da veia para a coleta de sangue a vácuo. A assepsia deve ser feita com movimentos circulares do centro para fora, com a utilização do antisséptico e uma gaze, deixando secar por 30 segundos, sem abanar nem soprar, além de não tocar mais no local.
Use um torniquete livre de látex para garrotear o paciente, posicionado-o de 7,5 a 10 cm acima do local escolhido para a punção. Tome cuidado para não apertar excessivamente ou exceder um minuto. Após a coleta de sangue com seringa, o material é colocado em tubos para coleta previamente identificados e encaminhado junto do pedido ao laboratório.
PRÁTICA: Meio hipotônico, isotônico e hipertônico
Objetivo: Demonstrar a influência da concentração de sal (NaCL) na solução sobre a integridade das hemácias
Princípio:. Quando comparamos duas soluções e essas apresentam a mesma concentração de soluto, dizemos que ela é isotônica. Quando uma apresenta maior quantidade de soluto, ela é chamada de hipertônica. Por fim, temos a solução com menor quantidade de soluto, que é chamada de hipotônica.
Material: 2 ml de sangue com anticoagulante; Solução saturada de NaCl a 10%; Soro fisiológico ( sol. NaCl 0,9%); água; tubos de ensaio; pipetas; suporte para tubos; centrífuga
Método:
- Enumerar 3 tubos (A, B e C) colocando 3,5ml de água no tubo A; 3,5ml de soro fisiológico no tubo B; e 3,5ml da solução saturada de NaCL no tubo C.
- Adicionar 1 gota de sangue em todos os tubos (A, B e C), homogeneizar e deixar na bancada por 5 a 10minutos. Agitar
- Centrifugar todos os tubos a 1500 rpm por 5min, retirar delicadamente da centrífuga e observar se o sobrenadante está transparente (sem hemólise), suavemente rosa (hemólise parcial) ou vermelho (hemólise total);
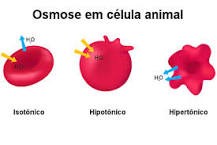
- Desprezar o sobrenadante e observar o sedimento (hemácias) em lâmina e lamíula, ao microscópio na lente de 40X; anotar as formas das hemácias ( integras, entumecida ou cremadas, conforme figura abaixo.
Interpretação: observação nos tubos
|
TUBOS |
MEIOS |
Sobrenadante |
Sedimento (hemácias) |
|
A (água) |
HIPOTÔNICO |
|
|
|
B (Soro fisiológico) |
ISOTÔNICO |
|
|
|
C ( Saturada NaCl) |
HIPERTÔNICO |
|
|
Sobrenadante: Transparente (sem hemólise), suavemente rosa (hemólise parcial) ou vermelho (hemólise total); SEDIMENTO (hemácias): integras, entumecida ou cremadas,
|
Ao microscópio observa-se as hemácias da seguinte forma: Hemácias integras no meio isotônico; Hemácias entumecidas hipotônico; Hemácias cremadas no meio hipertônico.
|
 |
Comentários:
Solução Isotônica: Uma solução isotônica é uma solução na qual a mesma quantidade de soluto e solução está disponível dentro da célula e fora da célula. A solução e a porcentagem de soluto são as mesmas dentro da célula que na solução fora da célula. Portanto, usando os números acima, uma célula colocada em uma solução de água com NaCl de 0,9% está em equilíbrio. Assim, a célula permanece do mesmo tamanho. A solução é isotônica em relação à célula.
Solução Hipertônica: Uma solução hipertônica é uma solução que contém mais soluto do que a célula que é colocada nele. Se uma célula com uma concentração de NaCl de 0,9% é colocada numa solução de água com uma concentração de NaCl de 10%, a solução é dita ser hipertônica. Hyper significa mais, o que significa que a solução em que a célula é colocada contém mais soluto do que a solução dentro da célula. Quando a solução contém mais soluto, isso significa que contém menos água. A solução fora da célula é 10% de NaCl, o que significa que é 90% de água. A solução dentro da célula é 0,9% de NaCl, o que significa que é 99,1% de água. Lembre-se, a solução flui de uma maior concentração de água para uma menor concentração de água. Isto é para diluir áreas com maiores concentrações de soluto, de modo que o equilíbrio possa ser alcançado. Sendo que a solução externa é de 90% de água, enquanto o interior contém 99,1% de água, a água flui do interior da célula para a solução externa para diluir as áreas altas da concentração de soluto. Portanto, a célula perde água e encolhe.
Novamente, quando fazemos referência a uma solução para dizer que é hipertônico ou hipotônico, estamos referenciando a quantidade de soluto presente na solução em comparação com o soluto dentro da célula que está na solução. Se a solução fora da célula tiver mais soluto do que a solução dentro da célula, a solução é hipertônica. Se a solução dentro da célula tiver mais soluto do que a solução fora da célula, a solução é hipotônica. Se a solução fora da célula contém o mesmo soluto que a solução dentro da célula, a solução é isotônica.
Solução Hipotônica: Uma solução hipotônica é uma solução que contém menos soluto que a célula que é colocada nele. Se uma célula com uma concentração de NaCl é colocada numa solução de água destilada, que é água pura sem substâncias dissolvidas, a solução no exterior da célula é 100% de água e 0% de NaCl. Dentro da célula, a solução é 99,1% de água e 0,9% de NaCL. A água, novamente, passa de uma concentração mais alta para uma concentração mais baixa para dissolver a concentração de soluto para alcançar o equilíbrio. Assim, a água vai da solução de água destilada para o interior da célula para diluir a concentração de soluto dentro da célula. Como consequência, a célula inunda e, possivelmente, explode. Assim, colocar uma célula com soluto em uma solução de água destilada causará inchaço e possível estouramento da célula.
PRÁTICA: DETERMIAÇÃO DA VELOCIDADE E DO TEMPO DE EFUSÃO DE DROGAS
Objetivo: Determinar da velocidade e o tempo de efusão de drogas
Princípio:. Efusão é um fenômeno físico que consiste na travessia de um líquido ou gás por orifícios existentes em um determinado recipiente (frasco de soro fisiológico) para outro sistema (corpo humano), impulsionada por um gradiente de concentração ou de força gravitacional. A velocidade é a razão entre o volume (ml) escoado pelo tempo (min.).
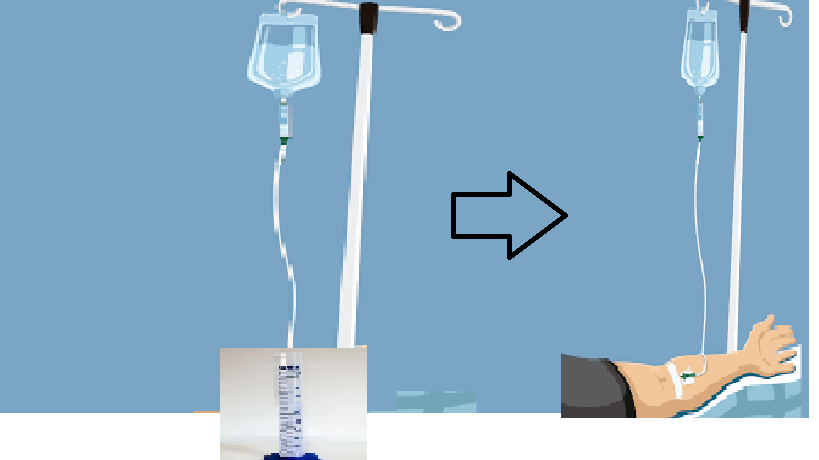
Material: Equipo acoplado a um frasco de soro fisiológico, suporte, cronômetro, proveta de 100ml
|
Método: acoplar um frasco de soro fisiológico a um equipo em um suporte em uma altura de pelo menos 60cm da bancada, conectado a uma proveta de 100ml; ajuste o regulador da evasão para cair 20 gotas/ml e determine o volume em 1 hora de evasão. Determine o tempo de evasão para escoamento de 500ml de soro e ajuste o escoamento para 120ml por hora. |
 |
Comentários:
O cálculo de medicamentos é de suma importância na área da enfermagem, pois através dele temos noção da quantidade de gotas por minuto a solução deverá ser infundida pelo horário prescrito. Vale lembrar que as instituições na sua maioria têm bombas de infusão onde é possível programá-la digitando volume e tempo que a medicação deverá ser infundida, porém em provas, concursos e até mesmo no caso de falha do equipamento é necessário saber realizar os cálculos (Coren, 2011).
QUESTÕES:
- Quais os fatores determinantes no tempo e velocidade de efusão de um medicamento?
- Qual o tempo necessário para efusão de 500ml de soro glicosado em sistema prescrito 20 gotas/min?
- Uma solução de 120 ml deverá ser infundida em 30 minutos EV. Quantas gotas por minuto serão administradas?
- Uma solução de 120 ml deverá ser infundida em 30 minutos EV. Quantas micro gotas por minuto serão administradas?
- Um paciente necessita de receber 250ml de sangue em uma transfusão que deve ser feita em 2 horas. Qual a velocidade de efusão?