Prof.Dr.Luis Carlos Figueira de Carvalho
Compostos de enxofre
1 INTRODUÇÃO
Os compostos com enxofre são metabolitos vegetais secundários derivados de aminoácidos. Caracterizam-se por apresentar vários aspectos comuns; dentre eles pode ser citado o uso das plantas que os contem como condimento e/ou alimento. As substancias com atividade biológica originam-se após a hidrólise de um precursor contido no vegetal pela ação de uma enzima encontram-se em compartimentos distintos no vegetal intacto, esta só entra em contato com o seu substrato após o rompimento das paredes celulares. Outra propriedade comum dos compostos com enxofre diz respeito das diferenças estruturais existentes entre eles, a grande maioria apresenta atividade antimicrobiana, tendo também sido descrita atividade protetora contra certas doenças degenerativas como o câncer e contra doenças cardíacas.
Existem duas classes de constituintes vegetais contendo enxofre de importância biológica. Uma dessas classes é caracterizada por tio-glicosídeos, também denominada glicosinolatos, que apresentam uma unidade de açúcar ligada a uma aglicona. Por hidrolise, através da enzima mirosinase, os glicosinolatos originam β-D-glicose e uma aglicona instável, que sofre rearranjo espontâneo com a perda de sulfato, originando um isotiocionato como produto majoritário, sendo esta a substancia responsável por grande número de atividades biológicas. A segunda classe de substâncias vegetais contendo enxofre é representada pela aliina, que ocorre principalmente no alho. A aliina, pela ação da enzima aliinase, origina a alicina que, juntamente com seus produtos de degradação, é responsável pelas atividades biológicas e pelo odor característico do alho.
6
2 DESENVOLVIMENTO
2.1 Propriedades químicas
Os glicosinolatos são classificados em alifáticos, aromáticos e indólicos, com base no aminoácido do qual derivam: metionina, fenilalanina e tirosina ou triptofano, respectivamente. Os principais tio-glicosídeos encontrados nos vegetais são a sinigrina, da mostarda-negra, a sinalbina, da mostarda-branca a gliconapina, da colza, além dos glicosinolatos contidos em vegetais comestíveis como o brócolis, o repolho e o nabo. Quando hidrolisados pela enzima mirosinase, estes originam issotiocianatos, nitilas, tiocianatos ou um composto similar (figura1). Em algumas plantas ocorre a transformação dos glicosinolatos em tiocianatos, podendo, estes últimos, originarem, por hidrólise, ácido tiociânico por hidrólise. Quando a hidrólise dos tio-glicosídeos se dá em pH 3 a 4, originam-se nitrilas. Em espécies como Brassica oleracea L. e Brassica napus L., entre outras, ocorrem tioglicosídeos cuja aglicona é alifática e apresenta um grupamento hidroxila em posição β. Após a hidrólise da ligação glicosídica, essas agliconas originam, espontaneamente, por cicatrização, as tioxazolidonas, também denominadas goitrinas, de atividade antitireoidiana (figura 2).

Figura 02: Formação de Goitrina a partir dos glucosinolatos
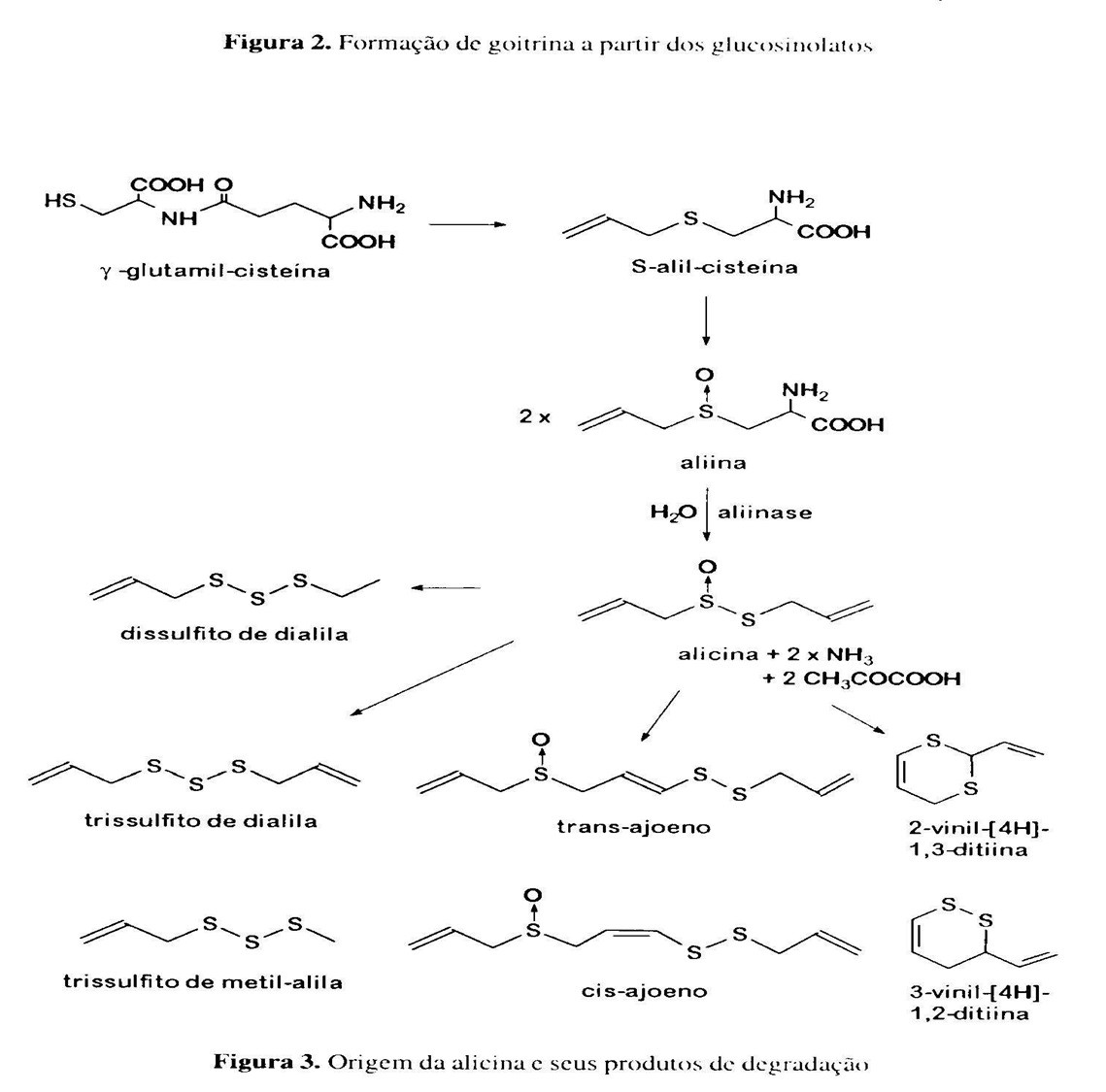
No caso do alho, as células intactas contem sulfóxido de (+)-S-alil-L-cisteína, composto inodoro, conhecido como aliina, que ocorre no bulbo em concetração em torno de 1% de peso fresco. Quando ocorre lise celular, a aliina entra em contato com a enzima aliinase, que se encontra estocada em vacúolos no interior das células e converte a aliina em alicina (tiossulfinato de dialila) (figura 3). Pela degradação da alicina e edição de alguns produtos de degradação originados na decomposição dessa substância, originando-se outros compostos com enxofre, como o cis- e o trans-ajoeno, a 2-vinil-[4H]-1,3-diitina e a 3-vinil-[4H]-1,2-diitina. Esses compostos também apresentam atividade biológica e podem ser isolados de preparações à base de alho (Reuter, 1990; Lawson, 1993; Sticher, 1991; Rosen et al., 2001).
2.2 Ocorrência e distribuição
Os glicosinolatos são encontrados exclusivamente em dicotiledôneas (Lawson, 1993), principalmente na ordem das Capparales. Têm uma distribuição limitada, tendo sido
8
encontrados em 16 famílias vegetais, destacando-se, entre elas, as famílias Brassicaceae, Capparidaceae, Resedaceae, Moringaceae e Tropaeolaceae. No âmbito farmacêutico destaca-se a família Brassicaceae, que inclui condimentos (mostarda) e vegetais utilizados como alimentos (brócolis, repolho, nabo), além de sementes oleaginosas importantes na agircultura (colza). A aliina e substancias relacionadas ocorrem na família Liliaceae, sendo particularmente abundantes no alho (Allium sativum L.). também ocorrem em espécies afins, como a cebola (Allium cepa L.) e alho-poró (Allium porrum L.) (Vannereau e Mellouki, 1996; Schulz et. Al., 1998).
2.3 Biogênese
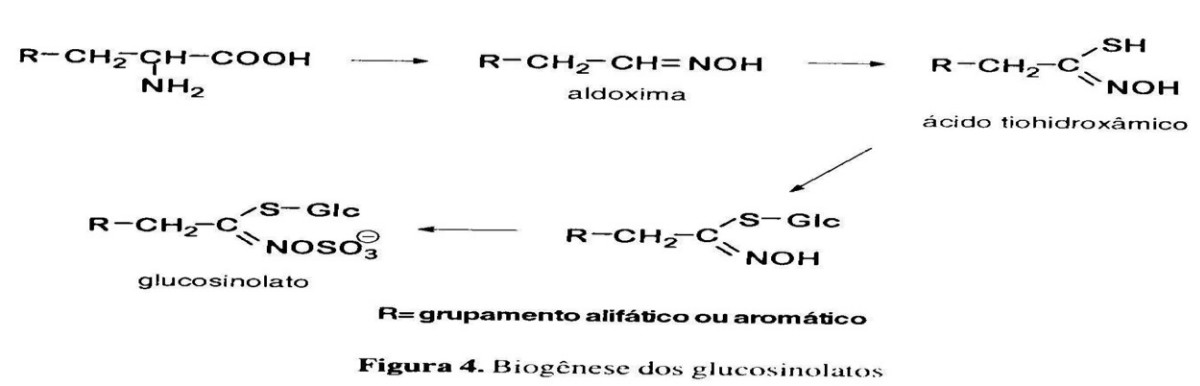
A biogênese dos glicosinolatos ocorre a partir de aminoácidos alifáticos e aromáticos (figura 4) e é conhecida por envolver oximas, tio-hidroximatos e dissulfoglicosinolatos como produtos intermediários. A rota biogenética principal atualmente aceita envolve N-hidroxilação e descaboxilação oxidativa, sendo que o primeiro passo origina uma aldoxima intermediária. Esta reação é comum entre os glicosinolatos e os heterosídeos cianogenéticos e é catalisada por enzimas homólogas do citocromo P450. Mais recentemente têm sido descritas rotas metabólicas alternativas para a biossíntese dos glicosinolatos, como, por exemple, a rota metabólica de alongamento da metionina e fenilalanina que, segundo Grser e.al., 2000, estaria envolvida na biossíntese dos glicosinolatos presentes em Brassica napus L. e Eruca sativa Mill.
O precursor da aliina no bulbo do alho é a γ–glutamil-cisteína. Essa substancia origina a S-alil-cisteína por hidrólise, que, por oxidação, dá origem à aliina (Lawson, 1993).
2.4 Atividades biológicas e emprego farmacêutico
Os glicosinolatos e seus produtos de degradação hidrolítica têm odor marcante e sabor pungente e apresentam uma série de efeitos biológicos envolvendo comunicação interespécies, que abrangem desde repelência química até a estimulação da ovoposição. Devido a estas atividades biológicas, alguns autores sugerem sua utilização no controle de pagas. São responsáveis pelas características organolépticas únicas de muitos dos condimentos que acentuam o sabor dos alimentos. Alguns produtos de hidrólise específicos também têm mostrado vários efeitos sobre o organismo humano (Mithen et. Al., 2000).
Os glicosinolatos propriamente ditos, tais como sinigrina, sinalbina e gliconapina, apresentam atividades biológicas sem muita importância, mas liberam produtos biologicamente ativos na degradação enzimática pela mirosinase em presença de água. Os compostos ativos originados podem ser isotiocianatos, cianetos orgânicos, oxazolidinotionas e tiocianatos iônicos, que são responsáveis pelos efeitos tóxicos de plantas pertencentes á família Brassicaceae frente a insetos, nematoides, fungos e mesmo outras plantas.
O interesse farmacológico principal do alho concentra-se atualmente na sua ação sobre a hipertensão, a arteriosclerose, agregação plaquetária e metabolismo lipídico, sistema imunológico e inibição da carcinogênese (Kannar et. Al., 2001; Yang et. Al., 2001).
2.5 Implicação do uso na alimentação
Pesquisas indicam que constituintes não-nutritivos contidos em vegetais utilizados na alimentação têm função importante na dieta como agentes protetores contra algumas doenças degenerativas. Dentre estes constituintes encontram-se os produtos de degradação dos glicosinolatos presentes em espécies de Brassica, bem como os produtos de degradação da alicina do alho (Dirch et. Al., 2000; Mithen et. Al., 2000; Shapiro et. Al., 2001).
2.6 Métodos de extração e obtenção
Os glicosinolatos são extraídos com álcool em ebulição (solução metanólica a 80 % ou etanol) a partir do tecido vegetal fresco. No caso dos glicosinolatos estarem contidos nas sementes, estas são pulverizadas e desengorduradas, seguindo-se extração em etanol ou metanol a 70%. Os glisinolatos também podem ser extraídos das plantas por homogeneização
10
dos tecidos vegetais com uma mistura de volumes iguais de dimetil-sulfóxido, dimetil-formamida e acetonitrila a -50°C. a purificação pode ser realizada por diversos métodos: colunas de troca iônica, cromatografia em papel com posterior eluição das manchas correspondentes, cromatografia sobre alumina. Mais recentemente têm sido desenvolvidos métodos de separação por cromatografia de interação hidrofílica e cromatografia iônica de fase reversa (Troyer et. Al., 2001).
Os isotiocianatos são obtidos do tecido vegetal triturado por destilação com vapor d’água ou por hidrólise ácida ou enzimática dos glicosinolatos. Neste caso, após a extração do material vegetal conforme descrito acima, o liquido extrativo é concentrado e o concentrado aquoso é então tratado pela mirosinase. Os isotiocianatos originados podem ser extraídos em éter etílico. Os isotiocianatos voláteis são separados por cromatografia gasosa, cromatografia em papel ou em camada delgada como derivados da tio-uréia. Outros produtos de transformação dos glicosinolatos, como as nitrilas, podem ser separados por CLAE preparativa. para a obtenção dos isiotiocianatos puros foi desenvolvida técnica utilizando a enzima mirosinase imobilizada em nylon, através da técnica de crosslinking (Leoni et. Al., 2000).
Aliina e seus produtos de transformação: a aliina é obtida a partir do alho fresco por extração com etanol a temperaturas inferiores a 0°C, enquanto que a alcina pode ser extarida em etanol diluído à temperatura ambiente; no entanto, devido à sua instabilidade, é de difícil isolamento. Os sulfitos podem ser separados a partir da fração volátil dos bulbos do alho por cromatografia gasosa (Harborne, 1984).
2.7 Métodos de doseamento
A sinalbina da mostarda-branca pode ser quantificada por titulometria, tendo sido desenvolvidos um método iodométrico e um método acidimétrico para este fim, enquanto que para a sinigrina foi otimizado um método de determinação por cromatografia iônica de fase reversa. A literatura também descreve a utilização de um método acidimétrico para a determinação quantitativa do isotiocianato da alila, presente na mostarda-negra. A oxidimetria também é adequada à quantificação desta substância, sendo a cloramina-T utilizada como agente oxidante. A determinação quantitativa dos isotiocianatos orgânicos pode ser realizada por espectroscopia no UV, após a ciclocondensação destes com dióis vicinais. A cromatografia gasosa pode ser utilizada para a determinação de nitrilas originadas a partir dos
11
glicosinolatos do brócolis. Para o doseamento da alicina, foram desenvolvidos inicialmente métodos titulométricos e colorimétricos para a determinação do enexofre total. A seguir passou-se a utilizar a cromatografia gasosa, muitas vezes acoplada à espectrometria de massas. No entanto, devido à instabilidade térmica da alicina, somente alguns de seus produtos de degradação, com as vinil-ditiinas e os sulfitos, podem ser determinados, sendo a quantificação da alicina realizada indiretamente. Atualmente, o método mais utilizado para a determinação quantitativa dos compostos com enxofre do alho é a CLAE, eventualmente acoplada a um espectrômetro de massas. A alicina pode ser determinada após a ação da aliinase imobilizada ou juntamente com a aliina por cromatografia iônica de fase reversa com detector UV do tipo fotodiodo. A CLAE também é o método de escolha para a determinação dos metabolitos do alho em fluidos fisiológicos e no ar expirado. A alicina também pode ser determinada por RMN, após derivatização, em preparações comerciais à base de alho (Miron et. Al., 1998).
2.8 Métodos de análise e caracterização
Os métodos cromatográficos são os mais utilizados para a análise dos compostos com enxofre. Além da cromatografia gasosa e da CLAE, também utilizadas na análise quantitativa, a literatura cita a cromatografia em papel e a cromatografia em acamada delgada sobre gel de sílica como métodos de análise adequados para esta classe de substâncias. Para a análise dos glisinolatos e dos isotiocianatos podem ser utilizados vários eluentes e diferentes métodos de detecção. Os constituintes do alho também podem ser analisados por cromatografia em camada delgada. Outra possibilidade para a análise de compostos com enxofre são os métodos espectroscópicos: ultravioleta, infravermelho, espectrometria de massas e ressonância magnética nuclear. Os glicosinolatos que ocorrem no estado sólido e cuja estrutura é conhecida podem ser caracterizados pelo ponto de fusão (Atahl e Schild, 1981).
2.9 Drogas vegetais clássicas
2.9.1 Mostarda
Nomes científicos: Brassica nigra (L.) W.D.J. Koch (Sinapis nigra L. e Sinapis alba L.);
Família botânica: Brassicaceae;
Parte usada: sementes de mostarda-negra ou alemã (Brassica nigra) e mostarda-branca ou amarela (Sinapis alba);
São empregadas as sementes maduras e secas das sílicas. As plantas são herbáceas e atingem até 1 m de altura. O óleo é obtido a partir das sementes moídas, após a expressão do óleo graxo/fixo, misturando-se o resíduo obtido com água e destilando-se por arraste de vapor d’água. Embora o conteúdo de óleo fixo destas sementes exceda a quantidade de óleo volátil originado pela hidrólise, este último é o responsável pelas atividades biológicas. A mostarda-branca é comercialmente tão importante quanto à mostarda-negra. Sua principal utilização também é como condimento, sendo que a mostarda-branca é mais suave do que a negra (Wagner, 1993, Robbers et. Al., 1996).
Emprego na alimentação: o fato da mostarda não conter colesterol e apresentar apenas traços de gorduras vegetais, classifica-a como condimento pouco calórico (1g de pó de mostarda equivale a 4,3 cal) e faz com que seja utilizada praticamente sem restrição para acentuar o sabor dos alimentos. Tradicionalmente, é utilizada também na medicina popular em algumas regiões, principalmente na forma de cataplasmas e compressas, devido às suas atividades antibacterianas e estimulantes da circulação sanguínea, neste último caso principalmente em regiões inflamadas.
Informações históricas: o uso da mostarda como condimento e planta medicinal remonta aos tempos da Grécia antiga. Com o passar dos séculos, foram criadas leis que protegiam os produtores de mostarda, garantindo assim a qualidade do produto. No inicio do século XVIII sua utilização decaiu, em parte por causa das novas especiarias provindas das Américas e do Oriente. Em 1856 o vinagre foi substituído pelo vinho no preparo da mostarda, o que resultou em uma especiaria menos ácida do que aquela consumida na França até então. Este condimento suave assumiu a partir daí o seu papel na história.
Dados químicos: a mostarda-negra contém cerca de 1% de sinigrina. O isotiocianato de alila, produzido a partir da hidrólise de sinigrina, é volátil e é comumente denominado óleo de mostarda. A mostarda-branca contém a sinalbina, que através da hidrólise origina isitiocianato de p-hidróxibenzila, de sabor pungente, não volátil e lacrimogêneo. Além de 2,5% de sinalbina, a
13
mostarda-branca também contém proteínas com atividade antimicótica, denominadas gama-tioninas, globulinas e óleos fixos/graxos. A alergia à mostarda-branca é causada por uma proteína com dois sítios alergênicos principais (Domíngues et. Al., 1990, Menéndez-Arias et. Al., 1990, Marcone et. Al., 1997).
Dados farmacológicos: das plantas que produzem glicosinolatos, as mostardas negra e branca são as de maior interesse farmacêutico, devido à atividade antibacteriana de seus constituintes. O espectro de ação destes engloba bactérias gram-positivas e gram-negativas, sendo o isotiocianato de benzila mais ativo do que o isotiocianato de alina. A atividade excitatória do óleo de mostarda sobre a musculatura é de natureza reflexa; além desta, apresenta efeitos inflamatório e irritante. Nos casos de inflamação, o óxido nítrico liberado pelo endotélio exerce função mediadora. Também foi relatado efeito antimicótico em casos de dermatofitose induzida em cobaias e atividade antioxidante (Abraham et. Al., 1975, Chung et. Al., 1997).
Precauções de uso: embora a mostarda seja consumida frequentemente, são raros os casos de hipersensibilidade descritos na literatura. A mostarda-negra é irritante local e emética; externamente, é rubefaciente. Tanto a mostarda-negra quanto a sinalbina, principal constituinte da mostarda-branca, tem atividade vesicante e o potencial de provocar reações alérgicas, eventualmente devido ao uso tópico, preconizado na medicina popular. São conhecidos casos de dermatite alérgica, de urticária e hipersensibilidade. Casos de reações alérgicas do tipo anafilático, em pessoas com hipersensibilidade à mostarda, também são descritos, sendo sugerido o mecanismo de hipersensibilização do tipo I. Hipersensibilidade especifica à mostarda dificilmente é detectada nos casos de manifestações alérgicas “idiopáticas” frente a alimentos industrializados, uma vez que, quase sempre, é omitida a composição total destes produtos (Moss, 1975, Kanny et. Al., 1995).
14
2.9.2 Brássica
Nomes científicos - Brassica oleracea L. e suas variedades:
Brassica botrytis L. subvar. cauliflora (Gars.) DC.: couve flor;
- var. botrytis L. subvar.. cymosa Lamk.: brócolis
- var. gongylodes L.: couve-rábano
- var. gemmifera DC,: couve-de-bruxelas
- var. capitata L.: repolho
- var. acephala L.: couve-manteiga
Brassica napus L. e suas variedades:
- var. arvensis (Lam.) Tell.: colza, canola
- var. napobrassica (L.) Peterm: nabo-branco
Brassica rapa L.: nabo-forrageiro
Raphanus sativus L.: var. radícula Pers.: rabanete
Eruca sativa Mill.: rúcula
Nasturtium officinale R. Br.: agrião
Família botânica: Brassicaceae
Partes usadas: diversas, como folhas, inflorescências, sementes e partes subterrâneas.
Emprego na alimentação: vegetais, como repolho, couve, couve-flor, couve-de-bruxelas, brócolis, rabanete, rúcula, agrião, entre outros, são utilizados na alimentação. A concentração em compostos com enxofre é maior nas inflorescências, variando significativamente de acordo com a estação em que se pretende cultivar e condições climáticas. A colza, a canola e o nabo são utilizados também na alimentação de animais domésticos. No caso da colza, os compostos com enxofre encontram-se nas sementes.
Dados químicos: dentre os cerca de cem diferentes glicosinolatos isolados até o momento, apenas 13 foram detectados em espécies comestíveis de Brassica; entre eles encontram-se glicoatropaeolina, sinalbina, sinigrina, glicobrassicina e glicorafanina. As enzimas que hidrolisam os glicosinolatos são produzidas por plantas e por organismos de ruminantes. Estas atuam sobre os glicosinolatos quando o tecido vegetal é triturado, por exemplo, na mastigação ou quando a
15
planta é consumida por um animal ruminante. Vegetais da família Brassicaceae também contêm ascorbigeno, composto derivado do ácido ascórbico, com propriedades imunomoduladoras, sendo seu processo de formação diretamente relacionado à concentração de glicobrassicina no material vegetal. Nastruzzi comprova que a transformação dos glicosinolatos em icotiocianatos e nitrilas são quantitativas, sendo os primeiros mais potentes no que se refere à inibição do crescimento de células tumorais.
Dados farmacológicos: a inclusão de espécies de Brassica na dieta parece ajudar a proteger contra o câncer de reto, cólon, pulmão, esôfago e leucemias. Os resultados dos testes farmacológicos até agora realizados indicam que alguns produtos de hidrólise dos glicosinolatos, como os indóis e os isotiocianatos, são capazes de induzir a atividade de enzimas da fase 1 e 2 de biotransformação, influenciando, assim, vários processos relacionados com a carcinogênese química, como o metabolismo, a atividade mutagênica e a capacidade dos agentes mutagênicos de se ligarem ao DNA. A concentração dos isotiocianatos, produtos de maior atividade frente às enzimas de biotranformação, é influenciada diretamente pelo processamento do vegetal durante a preparação dos alimentos. Além de inúmeros testes pré-clínicos realizados visando a comprovação da atividade protetora dos glicosinolatos e seus produtos de degradação frente à carcinogênese, recentemente têm sido realizados estudos de biodisponibilidade destes compostos em humanos. Os isotiocianatoa substâncias de maior atividade protetora contra o câncer in vitro, apresentam uma biodisponibilidade seis vezes maior que os glicosinolatos e sofrem conjugação com a glutationa in vivo, sendo metabolizados, originando o ácido mercaptúrico. Os metabólitos dos isotiocianatos recebem a denominação geral de ditiocarbamatos e podem ser detectados na urina. Paralelamente aos estudos químicos e farmacológicos, estão sendo realizadas as primeiras pesquisas visando o desenvolvimento de uma forma farmacêutica contendo glicosinolatos (Cortesi e. al., 2000).
Dados toxicológicos: os primeiros efeitos tóxicos descritos para os isotiocianatos e outros produtos da degradação dos glicosinolatos foram a inibição geral da absorção de iodo pela tireóide e a propriedade de provocar o aparecimento de bócio. Os efeitos sobre a tireóide foram comprovados em diversas pesquisas.
16
Estudos recentes, realizados com porcos e ovelhas, confirmaram a atividade dos glicosinolatos sobre o sistema endócrino, tendo sido detectado aumento nas concentrações plasmáticas de T3, T4, prolactina, progesterona e androstenediona. O período mais crítico para o desenvolvimento do hipotireoidismo foi durante a gravidez e a lactação, sendo que esta atividade também se manifestou sobre a prole, inclusive com a ocorrência de bócio congênito. No entanto, os efeitos antitireoidianos dos glicosinolatos mostraram-se reversíveis pela suplementação alimentar com iodo e selênio. Animais com dieta rica em colza apresentaram efeitos teratogênicos, tendo ocorrido também uma diminuição da fertilidade relacionada com a presença de glicosinolatos (Sharpe et. al., 1975; Mawson et. al., 1994).
Precauções de uso: embora quantidades excessivas de glicosinolatos consumidas por animais possam reduzir seu crescimento, além de afetar as funções da tireóide, fígado e rins, existem apenas evidencias mínimas destes efeitos sobre o organismo humano. Os trabalhos até agora realizados permitiram concluir que, em seres humanos, uma dieta diária estimada em 0,1 g de glicosinolatos somente pode ser considerada como um risco para a saúde nos casos de deficiência de iodo. A adição de quantidade extra de iodo na dieta pode ajudar a contrabalancear os efeitos antitireoidianos dos isotiocianatos, porém não atua sobre os efeitos das oxizolidino-2-tionas, que são produtos da hidrólise das tioxazolidonas. Pesquisas relativamente recentes permitiram o desenvolvimento de cultivares de colza, com baixos teores de glicosinolatos, como, por exemplo, a conola, que pode assim ser utilizada em quantidades elevadas na suplementação proteica do gado, sem os riscos apontados anteriormente. Os isotiocianatos de alila e fenetila, comumente encontrados em espécies comestíveis de Brassica, apresentam efeitos genotóxicos em testes realizados com bactérias in vitro. Ensaios posteriores, realizados com bactérias in vivo e na presença de homogenados de tecidos hepáticos, albumina sérica bovina e saliva humana, indicaram uma genotoxicidade consideravelmente menor, sugerindo que as substancias testadas sofram detoxificação pela ligação às proteínas. Os resultados obtidos até o momento não permitem concluir sobre o possível risco genotóxico para seres humanos, uma vez que os testes foram realizados em bactérias, in vitro e por curto período de tempo.
17
2.9.3 Alho
Nome científico: Allium sativum L.
Família botânica: Liliaceae.
Parte usada: bulbo maduro, fresco, formado por 6 a 15 dentes.
Dados químicos: a alicina, composto originado a partir da hidrólise da aliina, tem atividade antibacteriana potente. Decompõe-se rapidamente na presença de ar e água, originando dissulfito de dialila, trissulfito de dialila e o polissulfitos correspondes, todos apresentando um odor intenso. O dissulfito de dialila é o principal responsável pelo odor característico do alho. O mesmo processo de degradação ocorre no organismo, motivo pelo qual o ar expirado apresenta o mesmo após a ingestão. Além de conter aliina, o alho também contém proteínas, ácidos graxos, carboidratos, flavonóides, vitaminas A, B1, B2 e C, adenosina e saponinas esteroidais, tendo estas apresentado efeitos inibitórios sobre a coagulação sanguínea. A teoria mais aceita para explicar as atividades biológicas do alho baseia-se na reatividade apresentada pela alicina e por alguns de seus produtos de degradação frente a grupamentos sulfidrila de proteínas. Uma vez que foi mostrado in vitro que a alicina inibi um grande numero de enzimas, cujos sítios ativos contém cisteína, presume-se que os constituintes do alho contendo um grupamento di-tio-alila reagem com grupamentos sulfidrila de enzimas, bem como a acetil-CoA-SH, unidade fundamental na biossíntese do colesterol e dos triglicerídeos. Testes in vitro evidenciaram a alta permeabilidade da alicina através das membranas dos eritrócitos. Após sua penetração no organismo, a licina reage com a glutationa reduzida, cujo produto foi isolado e identificado e é o responsável pela inativação de enzimas contendo grupamentos SH. Recentemente foi desenvolvido um método de síntese para a alicina (Cruz-Villalon, 2001).
Dados farmacológicos: investigações farmacologiacs realizadas in vitro e in vivo indicaram para o alho atividades antibacteriana, antimicótica, antiviral, antiparasitária, antitumoral, antiflogística, imunomoduladora, antioxidante e fibrinolítica, além de inibição da agregação plaquetária e diminuição das taxas de
18
triglicerídeos e colesterol. A alicina atua contra bactérias patógenas gram-positivas e gram-negativas, incluindo alguns microrganismos resistentes a antibióticos. O efeito antimicrobiano principal da alicina é devido à sua reação química com o grupamentos tiol de várias enzimas como a álcool-desidrogenase, tiorredoxina redutase e RNA polimerase. Recentemente vários estudos demostraram a atividade do alho conta Helicobacter pylore. Ao contrario do que acontece com a maioria dos extratos vegetais, a atividade antimicótica do alho é mais intensa do que a sua atividade antibacteriana (Avato et. al., 2000).
A atividade anti-hipertensiva tem sido investigada e é atribuída à presença de peptídeos sulfurados, que atuariam aumentando os níveis fisiológicos de óxido nítrico. Ensaios clínicos controlados realizados em hipertensão, com produtos padronizados quanto ao teor de alicina, foram descritos por Grasberger (1997). Os resultados não foram conclusivos sobre a efetividade do alho como agente anti-hipertensivo, uma vez que os ensaios foram realizados com o número limitado de paciente e por curto espaço de tempo. Testes clínicos, realizados por Kalus et.al. (2000), evidenciaram uma efeito vasodilatador para o alho através da redução da pressão arterial, viscosidade plasmática e plaquetária e do hematócrito. Resultados de ensaios in vitro indicam um efeito vasodilatador para a alicina.
Um maior número de ensaios clínicos foi realizado em hiperlipidemias. A diminuição das taxas de triglicerídeos e colesterol foi constada em estudo clinico com pacientes hiperlipidêmicos, em um experimento controlado, sendo o tratamento realizado por 16 semanas com comprimidos de alho padronizados quanto ao teor de aliina. Uma meta-análise envolvendo 16 ensaios clínicos e um total de 952 pacientes indicou efetiva redução dos níveis séricos de colesterol e triglicerídeos; por outro lado, dois outros ensaios clínicos controlados indicaram ausência de eficácia. Dentre os estudos clínicos realizados recentemente, encontram-se aqueles que descrevem a redução dos níveis séricos de colesterol pelo alho em contraste com outros, cujos resultados indicam ausência desta atividade. Uma meta-análise, realizada por Stevinson et. al. (2000), levou os autores a questionarem o valor da utilização do alho no tratamento da hipercolesterolemia, uma vez que a diferença entre os grupos tratados e controles é modesta. Estudos de biodisponibilidade in vitro com comprimidos de revestimento entérico a base de alho, forma farmacêutica mais utilizada, detectaram uma baixa
19
taxa de liberação da alicina, devido à diminuição da atividade da aliinase, geralmente causada pelos adjuvantes dos comprimidos e/ou desintegração lenta destes. Por este motivo, estudos sobre a atividade biológica do alho só podem ser considerados validos quando a liberação de alicina dos comprimidos tenha sido determinada sob condições padronizadas. Ensaios in vitro, realizados visando determinar o mecanismo de ação hipocolesterolemiante dos constituintes do alho, indicam que a enzima esqualeno monoxigenase, que catalisa um dos passos limitantes da velocidade na biossíntese do colesterol, é um dos alvos destes compostos, sendo que sua inibição é lenta e irreversível, sugerindo uma ligação covalente à enzima. A alicina e o ajoeno também inibem a expressão da enzima óxido nítrico sintase induzível, presente nas lesões ateroscleróticas humanas e que provoca a ação do peróxi-nitrito, de ação deletéria.
A atividade antioxidante apresentada por extratos à base de alho e pela alicina pode ser explicada pela inativação de espécies reativas de oxigênio e pelo aumento de enzimas celulares antioxidantes como o superóxido-dismutase, a catalase, a glutationa-peroxidade e pelo aumento de glutationa nas células. Testes in vitro e in vivo indicam que a atividade antitumoral de preparados à base de alho é devida, principalmente, à estimulação de enzimas do citocromo P450, atividade antioxidante, aumento da apoptose e inibição de enzimas específicas das células tumorais. Outra explicação pode ser a atividade imunoestimulante do alho, uma vez que seus efeitos mostraram semelhança à imunoterapia po BCG (Lamm e Riggs, 2001).
Dados toxicológicos: os efeitos indesejados mais frequentes ocasionados pela utilização de produtos farmacêuticos a base de alho e também na sua utilização como alimento são as dermatites de contato. Pessoas alérgicas ao alho podem desenvolver uma erupção através do contato ou pela sua ingestão. Um trabalho experimental com teste de sensibilidade mostrou a ocorrência desta reação alérgica em cerca de 5% dos indivíduos testados. Os dados toxicológicos experimentais mais significativos advêm de experimentos realizados em hepatócitos de ratos: os resultados indicaram que, na presença de extratos de alho, ocorre um processo de detoxificação e uma ação antioxidante, mas também uma diminuição significativa da viabilidade celular, com alterações morfológicas importantes e diminuição da
20
atividade geral dos hepatócitos. Outro estudo também demostrou a citotoxicidade de extratos de alho, em culturas de hepatócitos. As pesquisas indicaram que o alho não apresenta genotoxidade nem cancerogenicidade e distúrbios de fertilidade ainda não foram realizados. Uma vez que o pó do alho causou lesões na mucosa gástrica, é aconselhável escolher a forma farmacêutica a ser administrada com cautela. A administração concomitante do alho com a varfarina, anticoagulante de ação indireta, pode provocar hemorragia (Fugh-Berman, 2000).
REFERÊNCIAS
ABRAHAM, A.: MOHAPATRA, L. N.; KANDHARI, K. C. et. al. The efects of some hair oils and unsaturated fatty acids on experimentally induced dermatophytosis. Dermatologica, v. 151, n.3, p. 144-148, 1975.
ACKERMANN, R. T.; MULROW, C. D..; RAMIREZ, G.; GARDNER, C.D.; MORBIDONI, L.; LAWRENCE, V. A. Garlic shows promise for improving some cardiovascular risk factors. Archives of internal Medicine, v.161, n. 6, p. 813-824, 2001.
ANÔNIMO, Mustard. Flavour Industry, v. 1, p. 596-598, 1970.
BALASENTHIL, S.; ARIVAHAGAN, S.; NAGINI, S. Effect of garlic on circulatory oxidant and antioxidant status during 4-nitroquinoline 1-oxide induced rat oral carcinogenesis. Nutrition Research, v. 20, n. 11, p. 1581-1589, 2000.
BLOCK, E. Biologisch active Organo-Schwefelverbndungen im Knoblauch. Deutsche Apotheker Zeitung, v. 28, n. 15, p. 3-4, 1989.
CHUNG, S. K.; OSAWA, T.; KAWAKISHI, S. Hydroxyl radical-scavenging effects of spices and scavengrs from brown mustard (Brassica nigra). Bioscience Biotechnology and Biochemistry, v. 61, n. 1, p. 118-123, 1997.
CISCA, E.; MARTYNIAK-PRZYBYSZEWSKA, B.; KOZLOWSKA, H. Content of glucosinolates in cruciferous vegetables grown at the same site for two years under different climatic conditions. Journal of Agricultural and Food Chemistry, v. 48, n. 7, p. 2862-2867, 2000.
GARDNER, C.D; CHATTERJEE, L. M.; CARLSON, J. J. The effect of a garlic preparation on plasma lipid in moderately hypercholesterolemic adults. Atherosclerosis, v. 154, v. 1, p. 213-220, 2001.